Nat Commun:小心!CRISPR/Cas9基因的编辑可能导致细胞毒性和基因组不稳定
- 2022-08-26 00:00
- 来源:医药资讯网
- 阅读:278
来源:100医疗网原创2022-08-26 1:45
CRISPR/Cas9俗称“基因剪刀”,是一种精准的基因编辑技术。它允许将所需的DNA序列引入(几乎)基因组的任何位置,从而修饰或失活基因。
CRISPR/Cas9俗称基因剪刀,是一种精准的基因编辑技术。它允许将所需的DNA序列引入(几乎)基因组的任何位置,从而修饰或失活基因。这项技术被广泛用于生物医学研究,一些基于CRISPR/Cas9的疗法正在进行临床试验,以治疗人类血液疾病、某些类型的癌症和艾滋病毒以及其他疾病。
在一项新的研究中,西班牙巴塞罗那生物医学研究所的研究员Fran Supek博士及其研究团队报告说,根据人类基因组的靶序列位点,CRISPR/Cas9基因编辑会导致细胞毒性和基因组不稳定性。这种不必要的影响是由关键的肿瘤抑制蛋白p53介导的,并由编辑位点附近的DNA序列和周围区域的几个表观遗传因素决定。相关研究结果于2022年8月4日发表在《自然通讯》杂志上,标题为crispr/cas 9切割的TP53依赖性毒性在基因组位点之间存在差异,可以证实遗传筛选。

使用计算方法,这些作者分析了为人类细胞设计的最受欢迎的CRISPR库,并检测到3300个显示强烈毒副作用的目标序列位点。他们还报告说,大约15%的人类基因包含至少一个显示毒副作用的编辑位点。
Supek博士解释说,我们的研究解决了与TP53相关的Cas9毒副作用的重要问题——这也是最近有争议的问题,它还提供了如何避免这一问题的方法。避免在这些风险网站进行编辑,不仅会使CRISPR编辑更加有效,更重要的是更加安全。
一个特定的基因可以在不同的位点进行编辑。论文的第一作者,巴塞罗那生物医学研究所的Miguel-Martin lvarez博士表示,基因中对调控重要或具有一些表观遗传标记的区域是最有可能触发p53反应的区域,因此作为一般建议应该避免。
P53介导的毒性和肿瘤发生
P53是一种被称为基因组卫士的蛋白质。它检测DNA损伤并指导细胞停止分裂,并可以导致程序性死亡,从而防止它们增殖和扩大其DNA中的错误。因此,p53是癌症和其他与DNA损伤相关的并发症的天然保护机制。
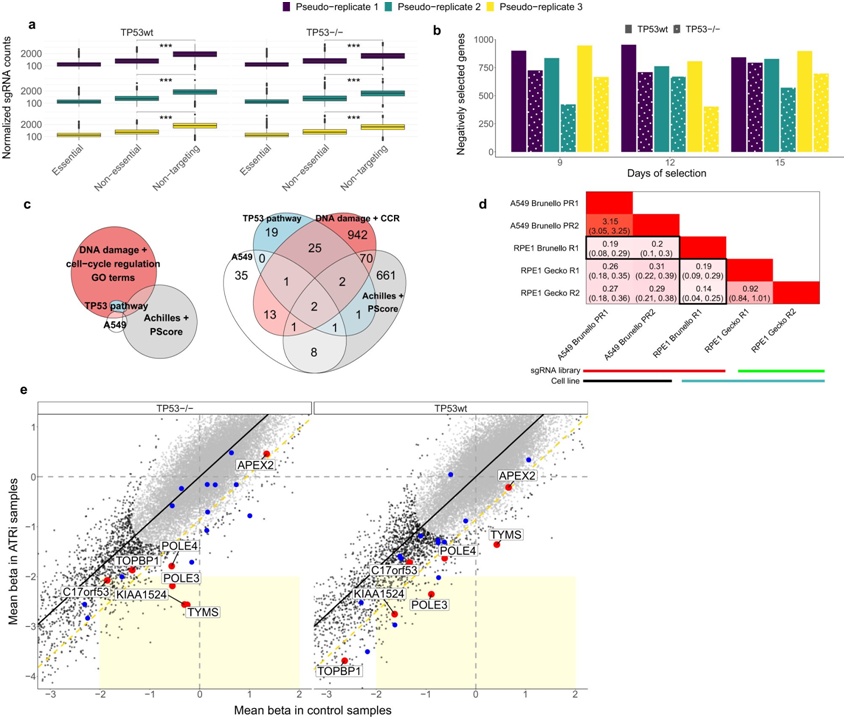
TP53野生型背景可能会混淆基因筛选中基因选择的估计。图片来自《自然通讯》,2022,doi :10.1038/s 41467-022-32285-1。
CRISPR基因编辑通常需要切割两条DNA链。在某些情况下,这种操作会触发p53反应,其中接受基因编辑的细胞会被标记为受损,然后被移除,从而降低基因编辑过程的效率。
然而,p53和基因编辑的主要并发症是,克服CRISPR编辑的细胞可能正是因为p53功能缺陷才这样做的。也就是说,这些细胞可能无法检测DNA损伤和/或标记细胞,然后随后遭受程序性死亡。因此,这种基因编辑方法最终可能会使基因组不稳定的细胞群体受益,这意味着他们容易积累进一步的突变,从而增加恶性肿瘤的风险。
Supek博士得出结论,这种不必要的后果可能会导致基因组不稳定的风险,这在体外CRISPR治疗中是非常不可取的,在体外CRISPR治疗中,患者的细胞在实验室中接受基因编辑,然后重新注入患者体内。我们希望我们的研究能够为如何设计更安全的CRISPR试剂提供一些指导,并鼓励在这个问题上的进一步研究。(100yiyao.com)
参考资料:
米格尔阿尔瓦雷斯等人。自然通讯,2022,doi :10.1038/s 41467-022-32285-1。
版权声明
本网站所有标注“来源:100医学网”或“来源:bioon”的文字、图片及音视频资料,版权归100医学网网站所有。未经授权,任何媒体、网站、个人不得转载,否则将追究法律责任。获得书面授权转载时,必须注明“来源:100医学网”。其他来源的文章均为转载文章。本网站所有转载文章都是为了传递更多信息。转载内容不代表本站立场。不想被转载的媒体或个人可以联系我们,我们会立即删除。
87%的用户都在使用100医疗网APP随时阅读、评论、分享、交流。请扫描二维码下载-

