《自然》子刊:浙江大学张丹团队揭示卵母细胞铁死亡在卵巢功能障碍发病机制中的作用和机制
- 2022-10-12 00:00
- 来源:医药资讯网
- 阅读:353
前期,张丹教授团队在一个涉及四代人的卵巢功能障碍中国大家族中,鉴定出一个与卵巢功能障碍相关的新基因突变:Basonuclin1(BNC1)基因的截短突变,(nm _ 001717.3: c . 1065 _ 1069 del/p . arg 356 valfs * 6)。转基因小鼠动物模型证实BNC1截短突变可导致卵巢功能障碍(Human Molecular Genetics,2018)。
本研究中,张丹教授团队进一步探索了BNC1基因截短突变导致卵巢功能障碍的具体调控机制。通过构建卵母细胞Bnc1特异性敲除的小鼠模型,发现BNC1主要通过干扰卵母细胞发育来影响小鼠卵巢储备。
现有Bnc1截短突变小鼠存在卵泡过早激活和闭锁衰竭,卵母细胞Smart-seq测序分析提示Bnc1截短突变小鼠存在脂质代谢和线粒体功能异常、Hippo途径和铁死亡途径异常。进一步发现Bnc1截短突变小鼠卵母细胞铁死亡相关指标水平异常,铁死亡相关表型被铁死亡激动剂RLS3诱导并加重,并可被铁死亡拮抗剂ferrostatin-1(Fer-1)逆转,提示Bnc1截短突变导致卵母细胞铁死亡。
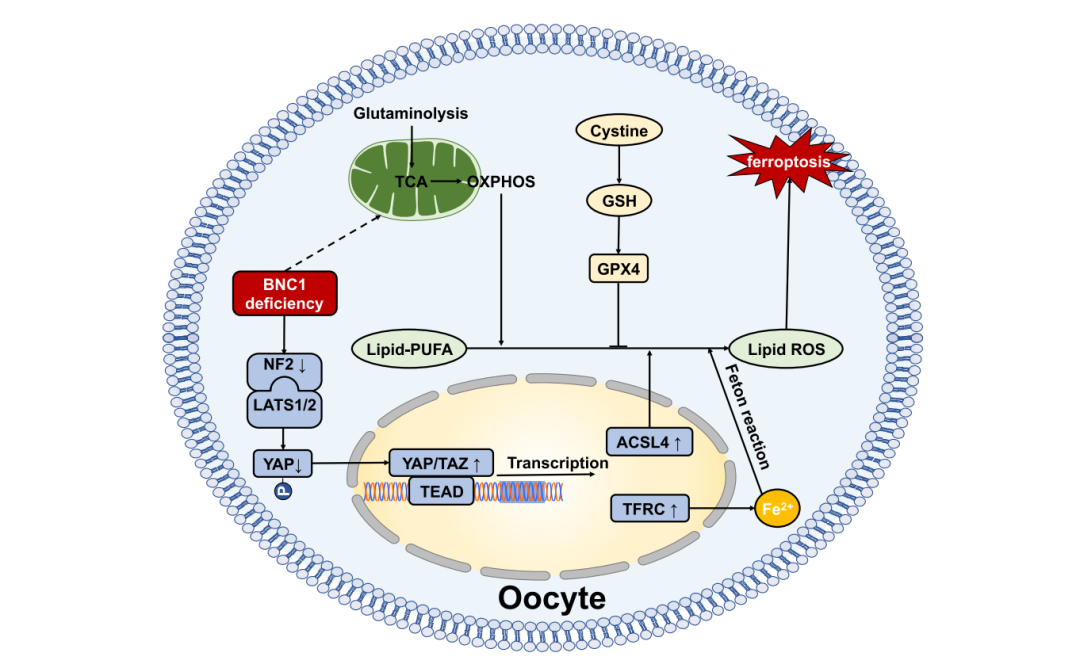
为阐明Bnc1截短突变诱导卵母细胞铁死亡的分子机制,张丹教授团队通过染色质沉淀测序(ChIP-seq)、ChIP-qPCR和双荧光素酶报告基因实验,发现并证实了BNC1的下游靶基因Nf2,阐明了NF2介导的Hippo-YAP-TFRC/ACSL4通路调控卵母细胞铁死亡的机制,并通过靶向NF2-YAP逆转了卵母细胞铁死亡引起的卵巢。