Cancer Cell:李博等开发机器学习算法,首次在单细胞水平追踪癌细胞和T细胞间线粒体传输
- 2023-10-13 00:00
- 来源:医药资讯网
- 阅读:217
来源:网络 2023-10-13 10:26
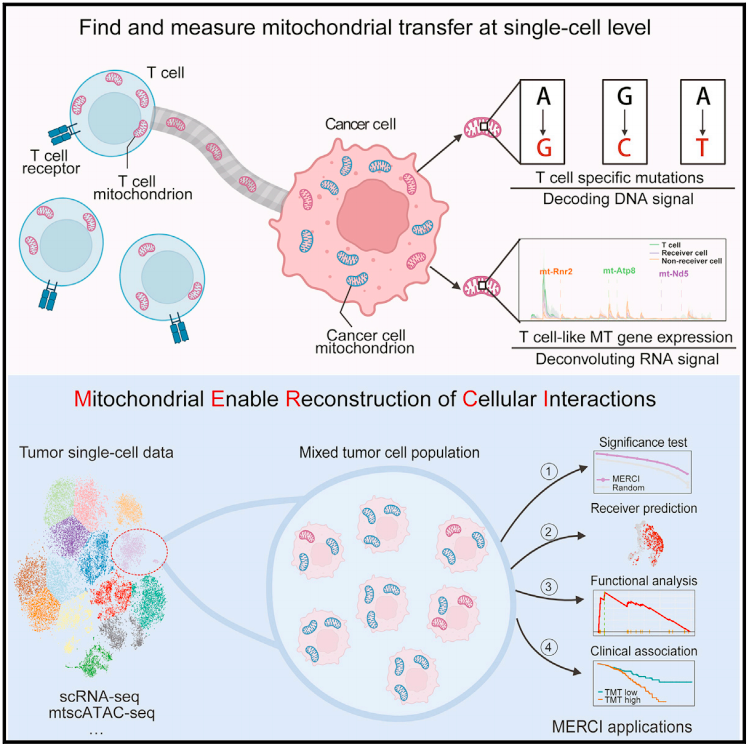
该研究不仅证实了T细胞与癌细胞间线粒体传输在不同癌症中的广泛存在, 更重要的是,提出了基于贝叶斯层次模型与统计反褶积的机器学习方法——MERCI,实现了在单细胞分辨率下追踪不同细胞间线粒体传输的重要功线粒体参与了真核细胞几乎所有的代谢活动(例如能量生成,信号传导以及细胞程序性死亡等),是哺乳动物在亚细胞层面最重要的 发动机 。线粒体可以通过细微的纳米管道在不同谱系的细胞间流动从而达到组织修复的目的, 这一生物学现象最早在2006年被观测确认。
2021年11月,哈佛大学医学院的研究人员在ure Nanotechnology期刊发表论文,首次发现,通过纳米管窃取T细胞的线粒体,在增强自身的同时,还削弱了细胞的活性,从而战胜免疫系统,实现免疫逃逸。该发现为的免疫逃逸以及T细胞的功能失调研究提供了全新的见解, 有很大希望成为新的癌症免疫治疗方向。
进一步的研究则需要在实验动物体内乃至真实癌症患者的肿瘤组织中进行,然而已有的生物学技术无法做到在体内追踪线粒体的运动轨迹。目前一个亟待解决的难点在于:没有现实可行的方法能在真实人类肿瘤中对癌细胞与T细胞间的线粒体传输进行研究并发现可药物靶向的关键基因和通路。
2023年10月9日,宾夕法尼亚大学医学院/费城儿童医院李博教授团队等在Cancer 期刊发表了题为:Systematic investigation of mitochondrial transfer between cancer cells and T cells at single-cell resolution的研究论文。
该研究不仅证实了T细胞与癌细胞间线粒体传输在不同癌症中的广泛存在, 更重要的是,提出了基于贝叶斯层次模型与反褶积的机器学习方法 MERCI,实现了在单细胞分辨率下追踪不同细胞间线粒体传输的重要功能。