AD:暨南大学发现全新阿尔茨海默病治疗靶点UBE2N!可有效降低Aβ积累、改善认知缺陷
- 2024-08-05 00:00
- 来源:医药资讯网
- 阅读:84
来源:奇点糕 2024-08-05 09:45
该研究发现,UBE2N的表达升高可能是导致AD患者脑内异常蛋白聚集的一个原因,而抑制UBE2N可改善AD病理,该结果也为揭示神经退行性疾病的分子机制及寻找药物靶点提供了新思路。近期,暨南大学殷鹏和李晓江团队发表了一项研究,他们在AD小鼠模型和AD患者大脑中发现,A 生成过程中会伴随着UBE2N水平升高的现象,而在AD小鼠模型和老年猴子大脑中,UBE2N过表达会加剧A 的沉积。
通过CRISPR/Cas9技术敲低UBE2N或使用UBE2N抑制剂可显著降低AD小鼠脑内A 的产生和积累,并改善小鼠的认知缺陷。
研究发表在Alzheimer s Dementia上[1]。

论文首页截图
为了观察UBE2N与A 病理之间的关系,研究人员首先对比了5-6个月大的5 FAD小鼠及野生型小鼠海马样本中UBE2N和K63的水平,结果在有A 沉积的5 FAD小鼠中发现了UBE2N和K63的水平明显增加的现象。
随后研究人员又在随年龄增长的APP/PS1小鼠和AD患者的大脑样本中观察到了同样的现象。这提示,A 生成过程中会伴随着UBE2N和K63水平升高的现象。
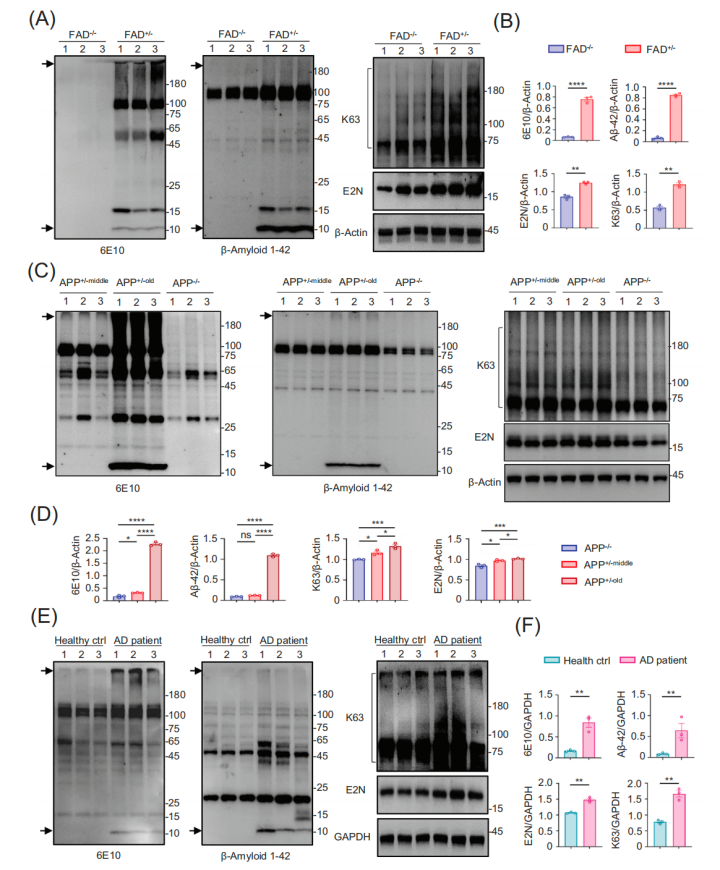
UBE2N和K63水平升高
进一步,研究人员将表达UBE2N或GFP(对照)的病毒载体注射到5-6个月大的5 FAD小鼠海马中,并在一个月以后进行了包括水迷宫、新物体识别等的认知功能测试。结果发现,UBE2N过表达会导致小鼠空间记忆能力显著受损。
蛋白印记等分析显示,与对照组小鼠相比,UBE2N过表达的5 FAD小鼠大脑中A 的聚集明显增加,这也证实了UBE2N过表达的确会促进A 病理。
随后,研究人员又在非人灵长类模型中对以上现象进行了再次验证,毕竟非灵长类模型常被用来观察老年动物的AD病理。
研究人员将表达人工A 42病毒载体与表达UBE2N病毒载体共同注射到不同年龄的食蟹猴右脑皮层中,对照组(A 42+GFP)注射到左侧。
病毒表达2个月后,研究人员发现,在老年猴(21-23岁)的大脑皮层中,UBE2N过表达可造成A 的产生,而在中年猴(7-9岁)或对照组中则没有A 产生。
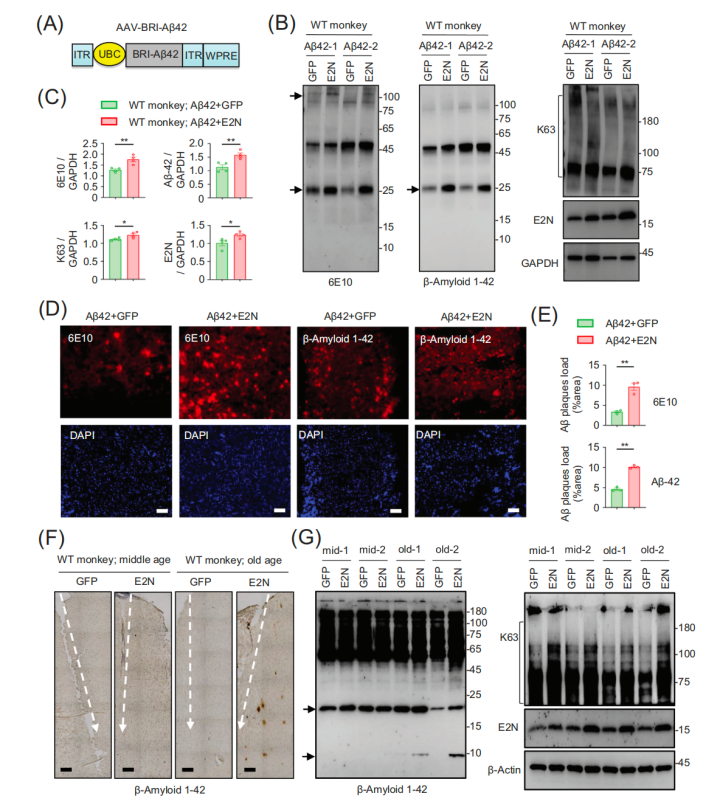
UBE2N促进老年猴大脑中A 的产生
鉴于UBE2N可介导k63的泛素化,因此,研究人员认为,在5 FAD小鼠和老年猴的大脑中,UBE2N可通过K63泛素化修饰影响A 的积累,从而加剧AD病理和认知缺陷。
既然UBE2N过表达会加剧AD病理,那么研究人员提出假设,即降低UBE2N水平或许可以通过泛素-蛋白酶体系统(UPS)途径清除A 来改善AD病理。因为正常情况下,UPS会通过正常泛素过程(K48泛素化)对错误折叠蛋白进行降解。
于是,研究人员CRISPR/Cas9技术敲低了5 FAD小鼠海马中UBE2N的表达,并在1个月后进行一系列认知行为测试。
结果显示,UBE2N敲低后,5 FAD小鼠认知行为得到明显改善。蛋白印记分析显示,敲低UBE2N后,K63水平明显降低,K48水平明显增加,A 聚集明显减少。也就是说,敲低UBE2N可通过增加K48泛素化来减少了A 的生成,并改善小鼠的认知障碍。
最后,研究人员还测试了一种UBE2N抑制剂,NSC697923。通过将其注入5 FAD小鼠海马后,研究人员发现,NSC697923可通过抑制K63泛素化,有效降低A 聚集。
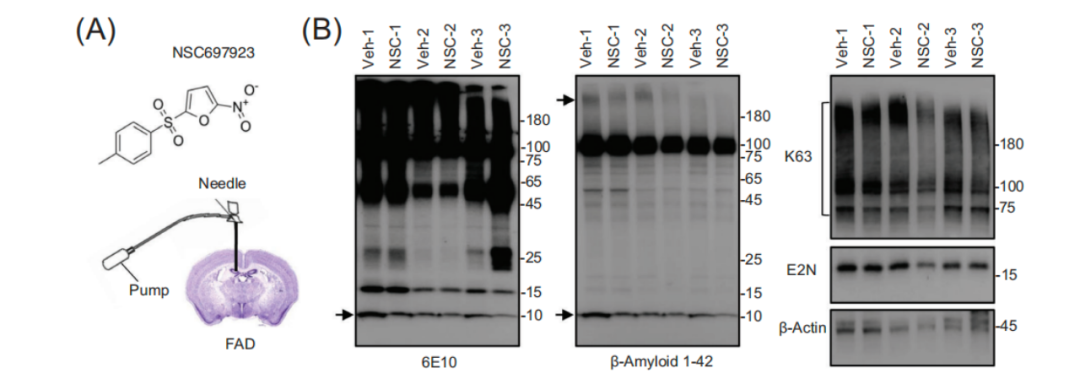
NSC697923改善A 病理
总之,该研究发现,UBE2N的表达升高可能是导致AD患者脑内异常蛋白聚集的一个原因,而抑制UBE2N可改善AD病理,该结果也为揭示神经退行性疾病的分子机制及寻找药物靶点提供了新思路。
版权声明 本网站所有注明“来源:100医药网”或“来源:bioon”的文字、图片和音视频资料,版权均属于100医药网网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:100医药网”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。 87%用户都在用100医药网APP 随时阅读、评论、分享交流 请扫描二维码下载->
