Sci Trans Med:夏伟梁、陆舜团队合作揭示PTPRT缺失增强非小细胞肺癌抗肿瘤免疫疗效
- 2024-09-14 00:00
- 来源:医药资讯网
- 阅读:483

在该研究中,研究团队通过对公共数据库分析和临床样本验证,发现携带T 型受体蛋白酪氨酸磷酸酶(PTPRT)基因突变特别是磷酸酶片段突变的患者更能从ICI治疗中获益。此外,PTPRT蛋白表达阴性的患者也是ICI治疗的响应人群。由此提出肿瘤PTPRT缺失是独立于PD-L1表达的预测ICI疗效的新型生物标志物。
研究团队通过转录组蛋白组测序、分子模拟和蛋白互作等实验阐明了分子机制:PTPRT 缺失型肿瘤表现出累积的 DNA 损伤、增加的胞质 DNA和更高的肿瘤突变负荷,间接激活STING通路。同时,鉴定出PTPRT去磷酸化的新底物为STING Y240位点。肿瘤PTPRT缺失提高了STING Y240位点酪氨酸磷酸化水平,抑制了STING的泛素化降解。
研究团队进一步发现PTPRT缺失的肿瘤通过激活 STING通路分泌更多的I型干扰素和趋化因子,增加肿瘤微环境中CD8+T细胞和NK细胞的浸润,使 冷 肿瘤转 热 ,增强了免疫检查点抑制剂在多种小鼠肿瘤模型中的治疗效果。
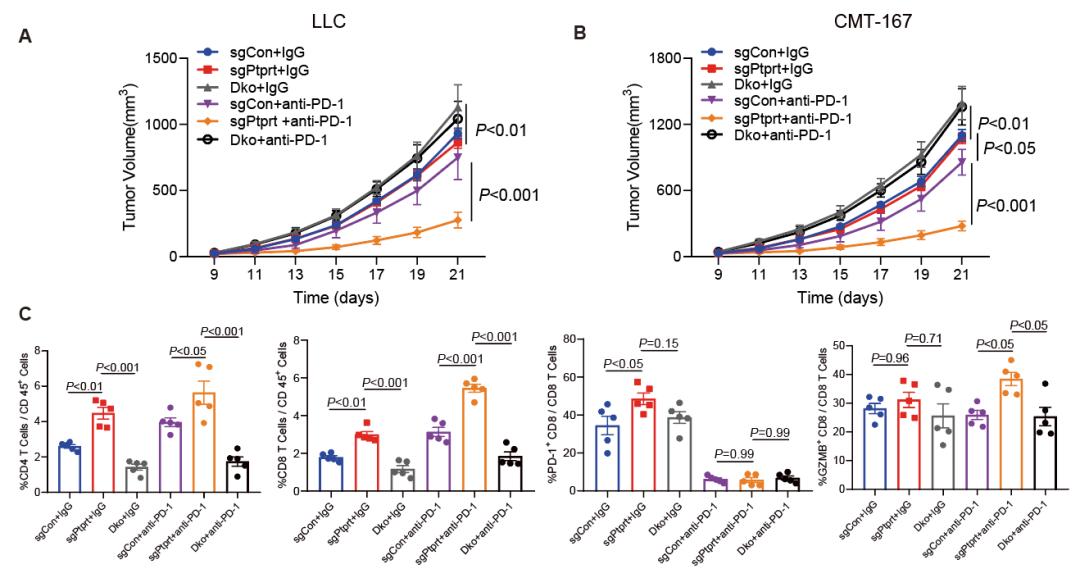
图1 肿瘤PTPRT缺失改善肿瘤免疫微环境,抑制肿瘤增长(Credit:Science Translational Medicine)
STING通路的激活在肿瘤免疫中是一把双刃剑:STING的激活不仅促进T细胞浸润和杀伤,同时也被证明诱导免疫抑制分子如PD-L1和IDO的表达,高剂量的STING激动剂可诱导T细胞凋亡【5】。STING蛋白在全身多种细胞中广泛表达,STING激动剂全身给药会诱导体内大量促炎因子的分泌,甚至引发细胞因子风暴【6】。基于 PTPRT 对 STING 的翻译后修饰机制,PTPRT 缺失通过延缓 STING蛋白的降解不会过度激活STING,也不上调免疫抑制分子PD-L1的表达。因此,抑制PTPRT是一种有前景的策略来增强抗肿瘤免疫。
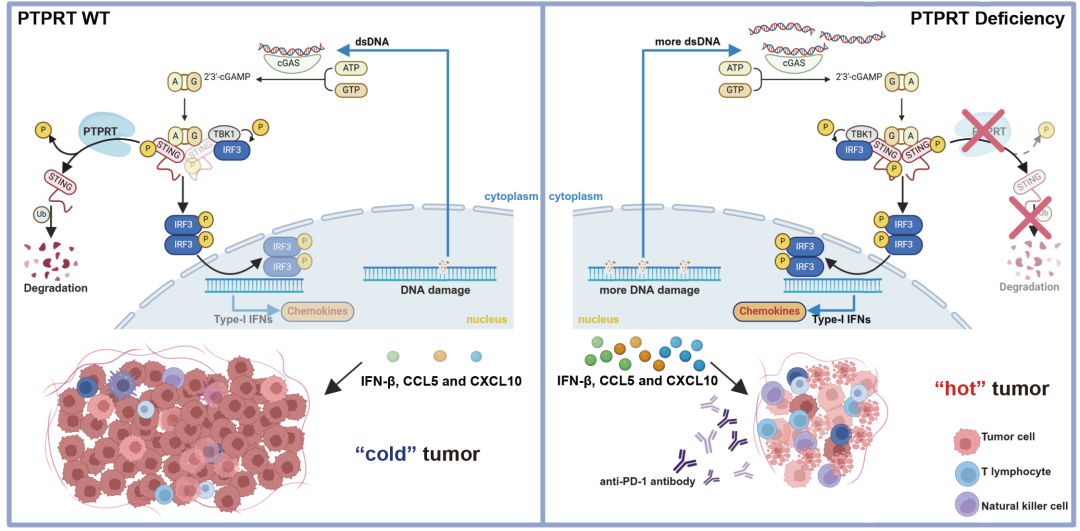
图2 研究示意图:肿瘤PTPRT缺失通过调节STING通路增强免疫检查点抑制剂疗效(Credit: Science Translational Medicine)
