自然共同体:科学家发现胰腺癌的潜在治疗靶点
- 2022-04-20 00:00
- 来源:医药资讯网
- 阅读:410
来源:100医疗网原创2022-04-20 14:41
胰腺导管腺癌(PDAC)是一种高度致命的疾病,其5年存活率低于9%。预计到2030年,它将成为癌症死亡的第二大原因。这项研究发现USP25是胰腺导管腺癌的潜在治疗靶点。
胰腺导管腺癌(PDAC)是一种高度致命的疾病,其5年存活率低于9%。预计到2030年,它将成为癌症死亡的第二大原因。PDAC肿瘤的侵袭性及其对传统化疗的耐药性被认为是由于缺乏临床靶向突变、细胞耗竭的缺氧微环境、代谢的改变和肿瘤的异质性造成的。泛素化酶(DUBs)在靶向蛋白质降解中发挥重要作用,代表了一种新的癌症治疗模式。然而,它们在胰腺导管腺癌(PDAC)中的治疗潜力还没有被探索。
近日,发表在《自然通讯》上的一篇题为《USP25促进病理HIF-1驱动的金属重编程,是胰腺癌Cer的潜在治疗靶点》的文章发现,USP 25作为PDAC肿瘤生长和活力所需的基本DUB,能够促进病理HIF-1驱动的代谢重编程,是一个潜在的治疗靶点。

在这项研究中,为了确定DUB的酶活性,研究人员开发了一种结合泛素-ABPs和质谱的分析管道,该管道将基于活性的蛋白质组学与患者来源的PDAC器官和小鼠遗传模型中的功能丧失遗传相结合。通过PDAC器官功能丧失的基因筛选确定了DUBs的功能意义,并且USP25被鉴定为PDAC肿瘤生长和活力所需的基本DUB。接下来,他们通过沉默其在KPCY样器官中的表达来评估Usp25的生物效应,并发现USP25的缺失导致器官样活力、存活率和体内PDAC肿瘤生长的下降。因此,USP25在PDAC的生长和维持中起着重要的作用。
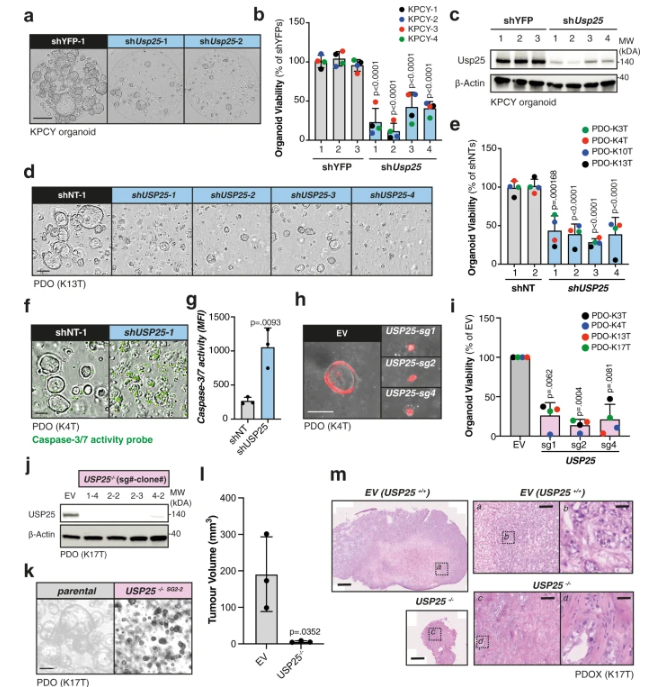
图25消耗USP25导致患者的器官样形成、活力和体内PDAC肿瘤生长减弱。
进一步发现,USP25通过调节HIF-1的稳定性和转录活性,是糖酵解的主要调节因子。为了评估Usp25在PDAC的作用,研究人员比较了它在PDAC和健康胰腺组织中的表达和酶活性。结果显示,与正常胰腺组织相比,USP25在PDAC具有高表达和酶活性,这与患者的低存活率有关。此外,遗传和药理学USP25抑制导致PDAC器官的强烈生长障碍,而正常胰腺器官不敏感,并导致来自患者的异种移植物的急剧退化。在机械上,USP25可以去泛素化并稳定HIF-1转录因子。PDAC的特点是严重的缺氧微环境,USP25的消耗会使HIF-1转录活性失效,破坏糖酵解,从而诱导肿瘤缺氧核心的PDAC细胞死亡。因此,USP25/HIF-1轴是PDAC代谢重编程和存活的基本机制,可用于治疗。
总之,这项研究发现USP25是胰腺导管腺癌的潜在治疗靶点。
参考文献:Nelson,J.K .Thin,M.Z .Evan,t .等USP 25促进病理HIF-1驱动的代谢重编程,是胰腺癌的潜在治疗靶点。国家通讯13,2070 (2022)。
版权声明
本网站所有标注“来源:100医学网”或“来源:bioon”的文字、图片及音视频资料,版权归100医学网网站所有。未经授权,任何媒体、网站、个人不得转载,否则将追究法律责任。获得书面授权转载时,必须注明“来源:100医学网”。其他来源的文章均为转载文章。本网站所有转载文章都是为了传递更多信息。转载内容不代表本站立场。不想被转载的媒体或个人可以联系我们,我们会立即删除。
87%的用户都在使用100医疗网APP随时阅读、评论、分享、交流。请扫描二维码下载-

