中山大学曹楠团队提出体细胞重编程与心脏再生修复新策略
- 2022-04-30 00:00
- 来源:医药资讯网
- 阅读:234
人心没有大人,已经成了学术圈。心血管祖细胞(Cardiovascular祖细胞,CPCs)出现在胚胎发育阶段,是目前唯一公认的具有体内心肌分化能力的干细胞,具有血管平滑肌细胞和血管内皮细胞的分化潜能,因此在心脏再生方面具有广阔的应用前景。移植到梗死心脏后,CPCs不仅可以补充受损的心肌细胞,还可以通过分化为毛细血管改善梗死区的血液循环,促进内源性和外源性心肌细胞的存活。许多研究证明,CPCs移植能显著改善心肌梗死后的心功能,且比单纯心肌细胞移植效果更显著、更持久。因此,CPCs作为心脏替代治疗最有前途的供体细胞之一,已显示出广阔的临床应用前景。然而,CPCs只存在于胚胎发育阶段,因此如何从成体中获得并扩增CPCs细胞成为亟待解决的关键问题。
中山大学中山医学院的曹楠教授带领的团队在Nature Biomedical Engineering Journal(TOP,Area 1,中科院,IF='23.7)发表了一篇论文,题目是在无氧条件下通过小分子将纤维重编程为可扩增的心血管祖细胞。本研究首次利用小分子化合物的组合,将小鼠和人成纤维细胞重新编程为化学诱导的CPCs(ciCPCs),并实现其大规模扩增。CiCPCs移植入梗死心脏后可同时促进瘢痕区心肌重建和血管化,从而显著促进梗死心脏的修复和心功能的恢复。因此,从患者自体细胞中制备和扩增CPCs用于心脏修复的新策略被创造出来。
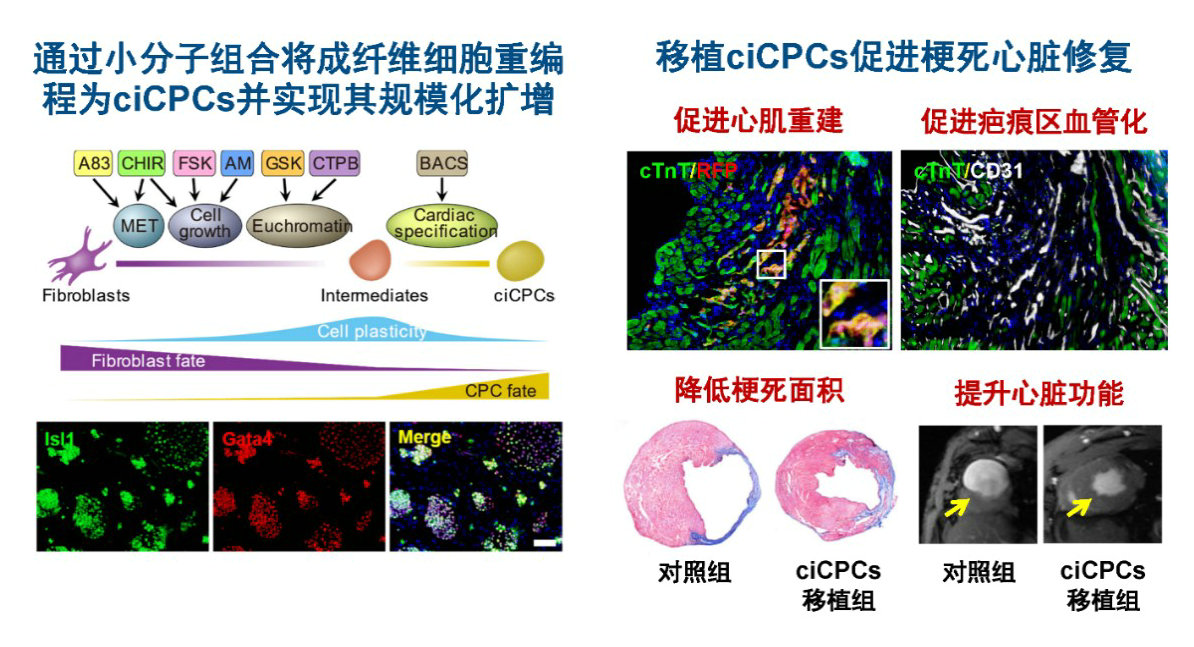
图:通过体细胞重编程获得的心血管祖细胞疗法
中山医学院著名副研究员王佳博士和顾珊珊博士是论文的第一作者。曹楠教授是这篇论文的通讯记者。本研究得到了国家重点科技攻关项目的资助。d计划、国家和广东珠江人才计划引进创新创业团队等项目。
